Master Pharmaceutical Medicine · Modul 4.1 · Teilzeit
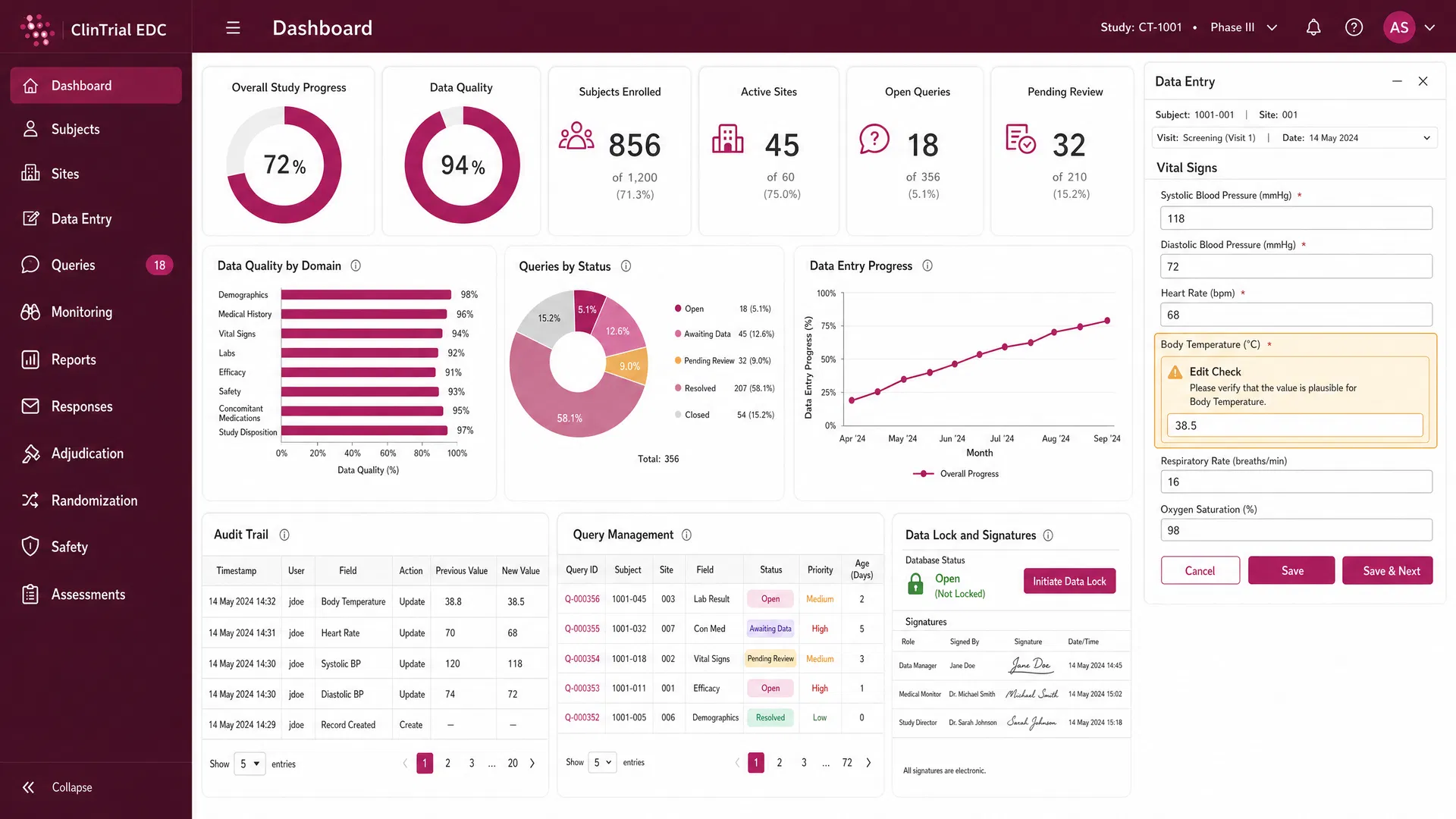
Clinical Systems & Data Management
Ein interaktives Lernmodul der Charlotte Fresenius Hochschule. Erlangen Sie ein tiefes Verständnis des Datenmanagements in klinischen Studien – von der Teamstruktur über CRF-Design bis hin zu modernen EDC-Systemen.
3
Module
~2 Std.
Gesamtdauer
Master
Niveau
Zertifikat
Abschluss
Lernziele des Kurses
Datenflüsse in globalen klinischen Studien organisieren
CRFs (Case Report Forms) nach Best Practices entwerfen
Edit Checks definieren und EDC-Systeme einsetzen
CDISC-Datenstandards (CDASH, SDTM) anwenden
Query-Management und Datenbereinigung durchführen
IT-Infrastruktur im Pharma-Umfeld verstehen
Regulatorische Anforderungen (GCP, 21 CFR Part 11) umsetzen
Interdisziplinäre Zusammenarbeit im DM-Team koordinieren
Kursmodule
Modul 1
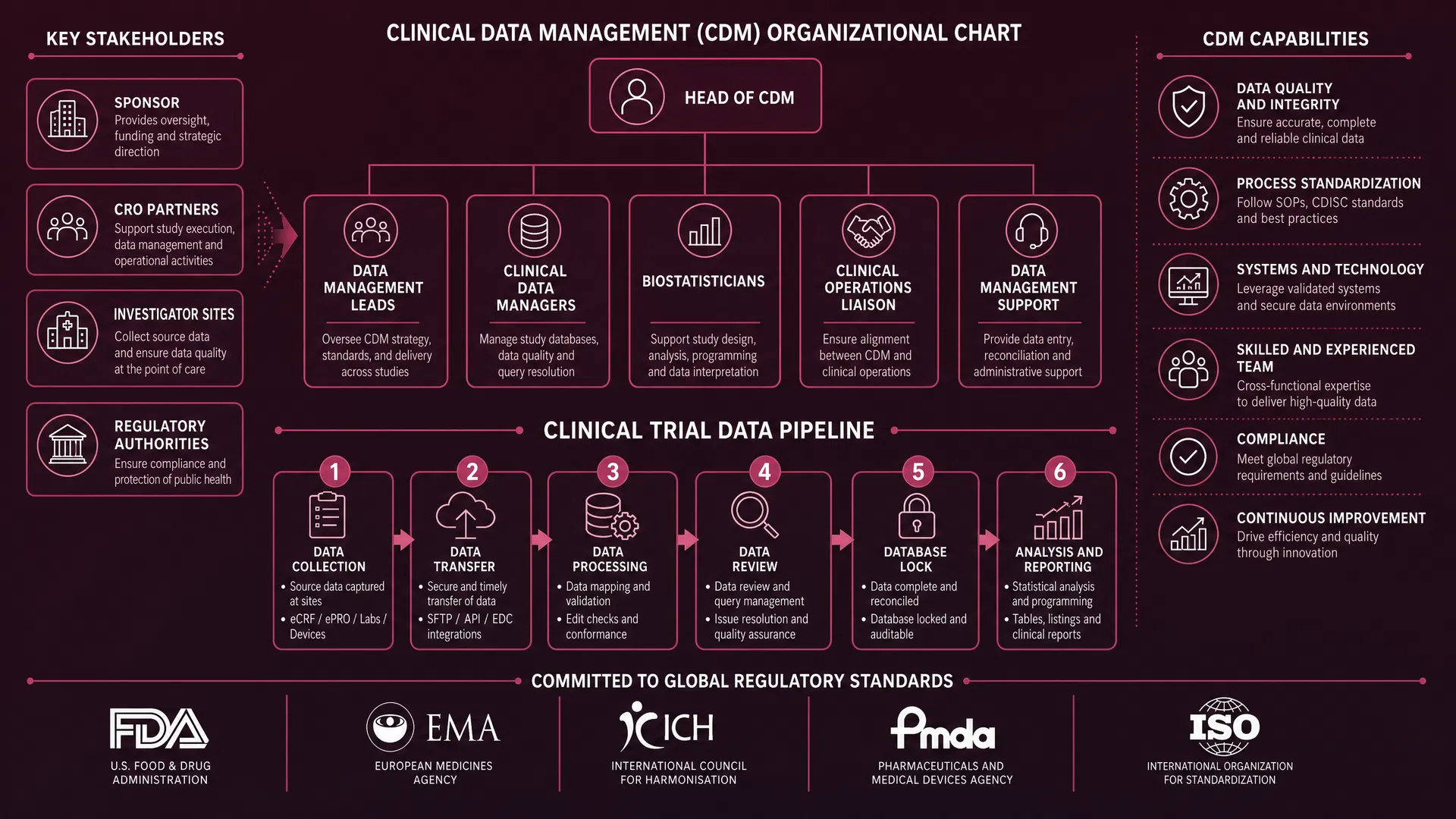
Globales Datenmanagement
Lernen Sie die Grundlagen des klinischen Datenmanagements: Teamstrukturen, Deliverables, regulatorische Anforderungen und Datenflüsse in globalen Phase-III-Studien.
DM-TeamGxP/ALCOA+21 CFR Part 11Datenfluss
~40 Min.
Modul 2
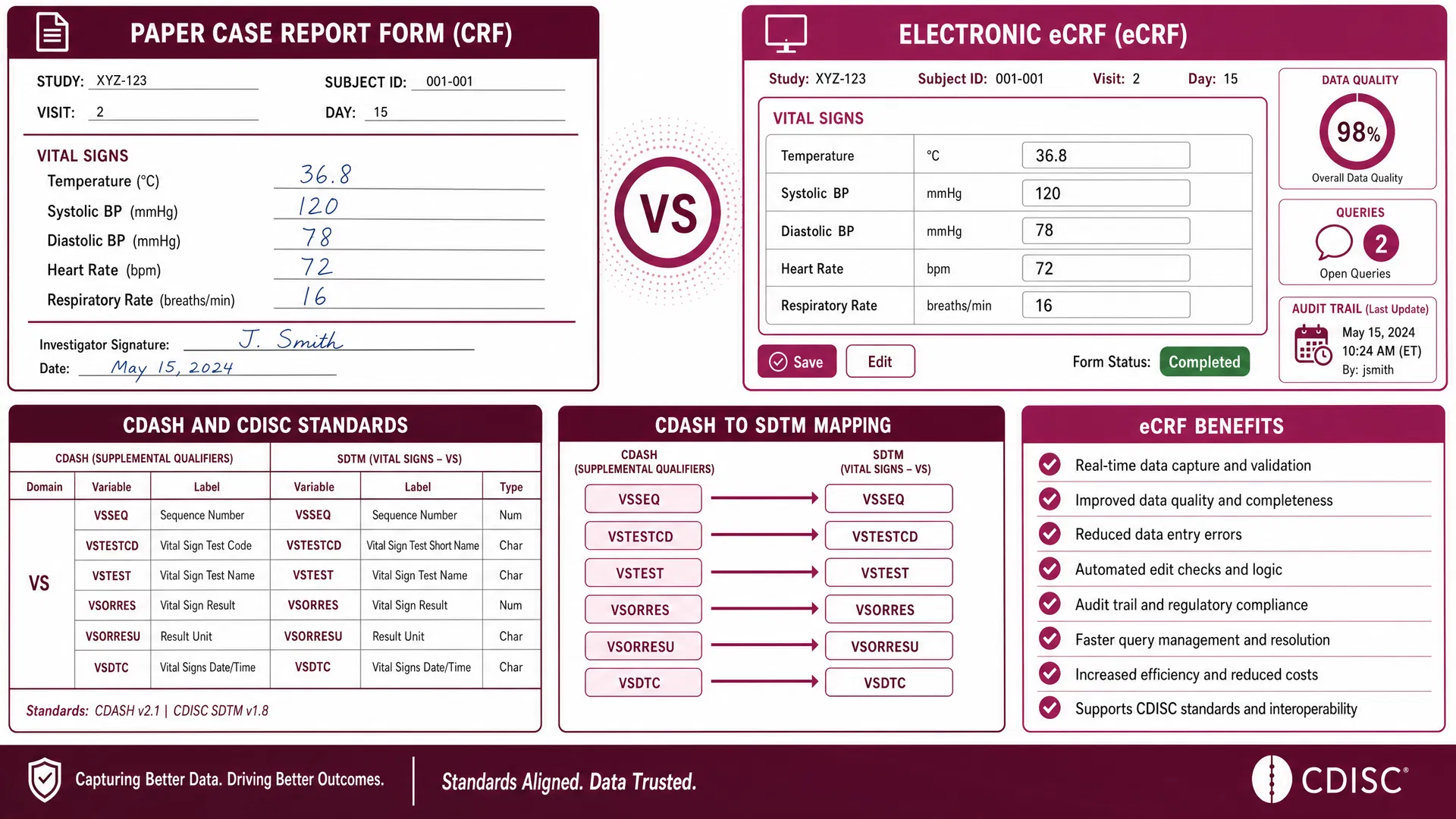
Case Report Form (CRF)
Verstehen Sie die Prinzipien des CRF-Designs, CDISC/CDASH-Standards und die Unterschiede zwischen Papier-CRF und eCRF. Praktische Übung mit dem CRF-Builder.
Lean CRFCDASHeCRFICH/GCP
~40 Min.