Case Report Form (CRF)
CRF-Designprinzipien, CDASH-Standards und praktische Übungen
Lernziele dieses Moduls
- Grundprinzipien des CRF-Designs (Lean CRF) anwenden
- Den Zusammenhang zwischen Protokoll und CRF erklären
- ICH/GCP-Anforderungen an CRFs kennen
- CDASH/CDISC-Standards bei der CRF-Gestaltung berücksichtigen
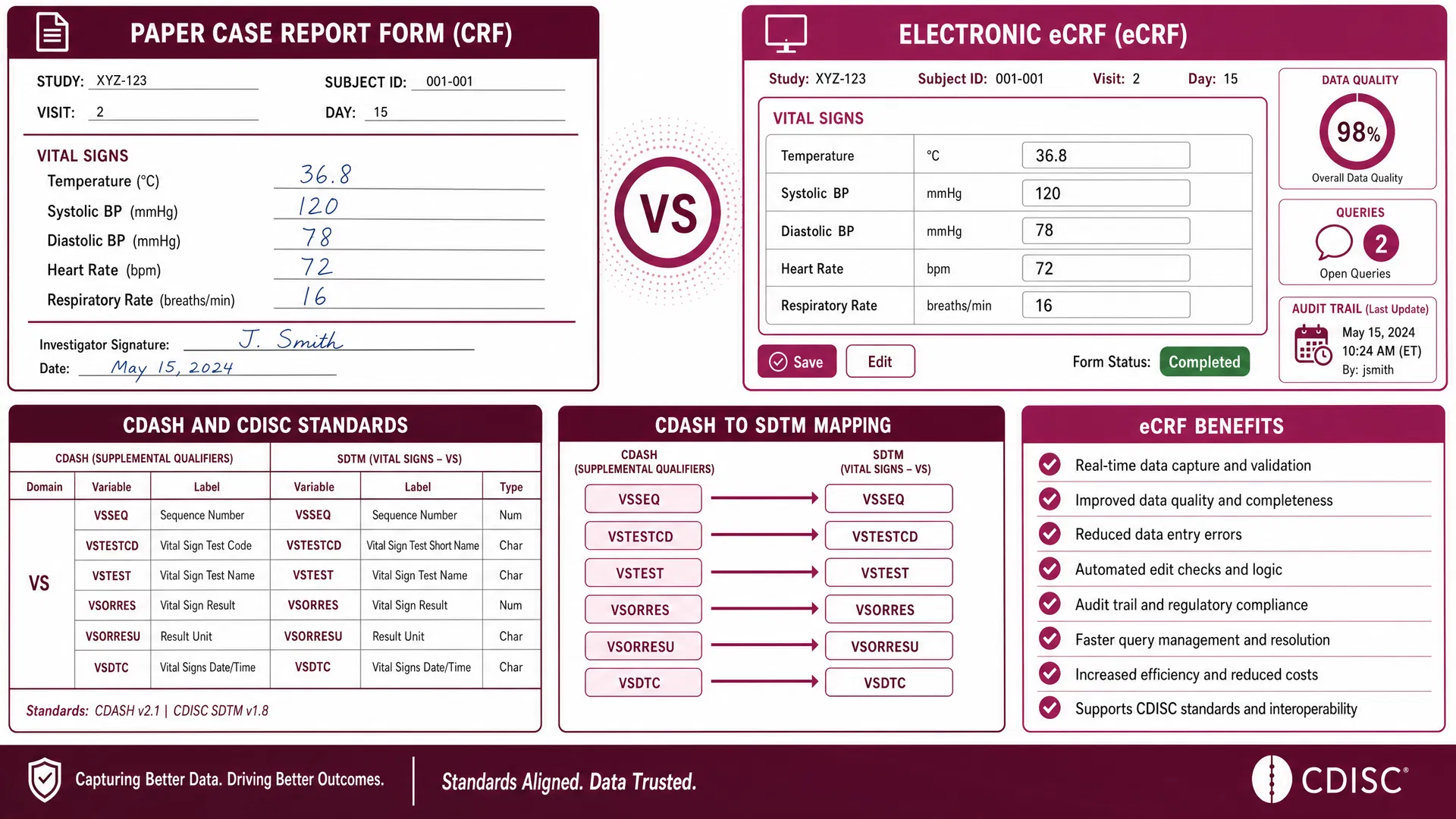
- Vor- und Nachteile von Papier-CRF vs. eCRF abwägen
Was ist ein Case Report Form (CRF)?
CRF Das Case Report Form (CRF) ist das zentrale Datenerfassungsinstrument einer klinischen Studie. Es enthält alle studienrelevanten Patientendaten, die gemäß Protokoll erhoben werden müssen.
Ein gut gestaltetes CRF ist entscheidend für die Datenqualität: Es minimiert Fehler, erleichtert die Dateneingabe und stellt sicher, dass alle für die Auswertung benötigten Daten vollständig und korrekt erfasst werden.
Lean CRF – Weniger ist mehr
Das Lean-CRF-Prinzip besagt: Erheben Sie nur Daten, die tatsächlich für die Studienauswertung benötigt werden.
Protokollgetrieben
Jedes CRF-Feld muss durch das Studienprotokoll begründet sein. Keine Daten ohne Auswertungsplan.
Eindeutig & klar
Fragen müssen unmissverständlich formuliert sein. Einheitliche Terminologie und klare Anweisungen.
Standardisiert
Verwendung von CDASH-Feldnamen und -strukturen für einfachere Datenverarbeitung und Behördeneinreichung.
Fehlerminimierend
Logische Struktur, sinnvolle Reihenfolge und klare Ausfüllhinweise reduzieren Datenfehler.
m2.gcp.title
m2.gcp.intro
m2.gcp.ich1Title
m2.gcp.ich1Desc
m2.gcp.ich2Title
m2.gcp.ich2Desc
Papier-CRF vs. eCRF
Papier-CRF
Pro
- Keine IT-Infrastruktur erforderlich
- Einsatz in ressourcenarmen Umgebungen
- Kein Systemausfall-Risiko
Contra
- Manuelle Dateneingabe fehleranfällig
- Kein Echtzeit-Monitoring
- Aufwändige Archivierung
- Kein automatischer Audit Trail
eCRF (Electronic CRF)
Pro
- Automatische Edit Checks
- Echtzeit-Datenzugriff
- Automatischer Audit Trail
- Integriertes Query-Management
- CDISC-konforme Datenstruktur
Contra
- IT-Infrastruktur erforderlich
- Systemvalidierung nach 21 CFR Part 11
- Schulungsaufwand
- Abhängigkeit von Internetverbindung
CDASH/CDISC-Standards
CDASH (Clinical Data Acquisition Standards Harmonization) ist der CDISC-Standard für die Datenerhebung auf CRF-Ebene.
Standardisierte Feldnamen
CDASH definiert einheitliche Variablennamen (z.B. VSORRES für Vital Signs Ergebnis), die direkt in SDTM-Datensätze überführt werden können.
Effizientere Einreichungen
FDA und EMA fordern CDISC-konforme Daten für Behördeneinreichungen. CDASH-konforme CRFs reduzieren den Aufwand für die Datentransformation.
Demographische Daten
Vitalzeichen
Unerwünschte Ereignisse
Begleitmedikation
Labordaten
Studienmedikation
Übung: CRF-Builder – Vital Signs
Entwerfen Sie einen Vital Signs CRF-Abschnitt. Wählen Sie die Felder aus, die Sie für eine kardiovaskuläre Studie benötigen.
Pflichtfeld für kardiovaskuläre Studien
Pflichtfeld für kardiovaskuläre Studien
Pflichtfeld
Standardfeld
Standardfeld
Optional, aber empfohlen
Optional
Pflichtfeld – ALCOA: Contemporaneous
Empfohlen für Blutdruckmessungen
Nur bei bestimmten Studiendesigns relevant
Wissenstest: Modul 2
Beantworten Sie alle 5 Fragen. Zum Bestehen sind 60% erforderlich.
Frage 1:Was ist das Hauptprinzip des 'Lean CRF'-Ansatzes?
Frage 2:Wofür steht CDASH im Kontext klinischer Studien?
Frage 3:Welcher CDASH-Domänen-Code wird für Vitalzeichen verwendet?
Frage 4:Was ist ein wesentlicher Vorteil des eCRF gegenüber dem Papier-CRF?
Frage 5:Was versteht man unter dem 'Protokoll-CRF-Verbindung'?