Überblick Globales Datenmanagement
Teamstrukturen, Deliverables, Schnittstellen und regulatorische Grundlagen
Lernziele dieses Moduls
- Die Rolle des Datenmanagements im Gesamtstudienprozess verstehen
- Typische DM-Organisationsstrukturen (Sponsor, CRO, Global/Lokal) kennen
- Wichtige Deliverables (DMP, TMF, Cleaned Database) benennen und erklären
- Schnittstellen des DM-Teams zu anderen Abteilungen beschreiben
- Regulatorische Grundlagen (GxP, FDA 21 CFR Part 11, ALCOA+) anwenden
Was ist Clinical Data Management?
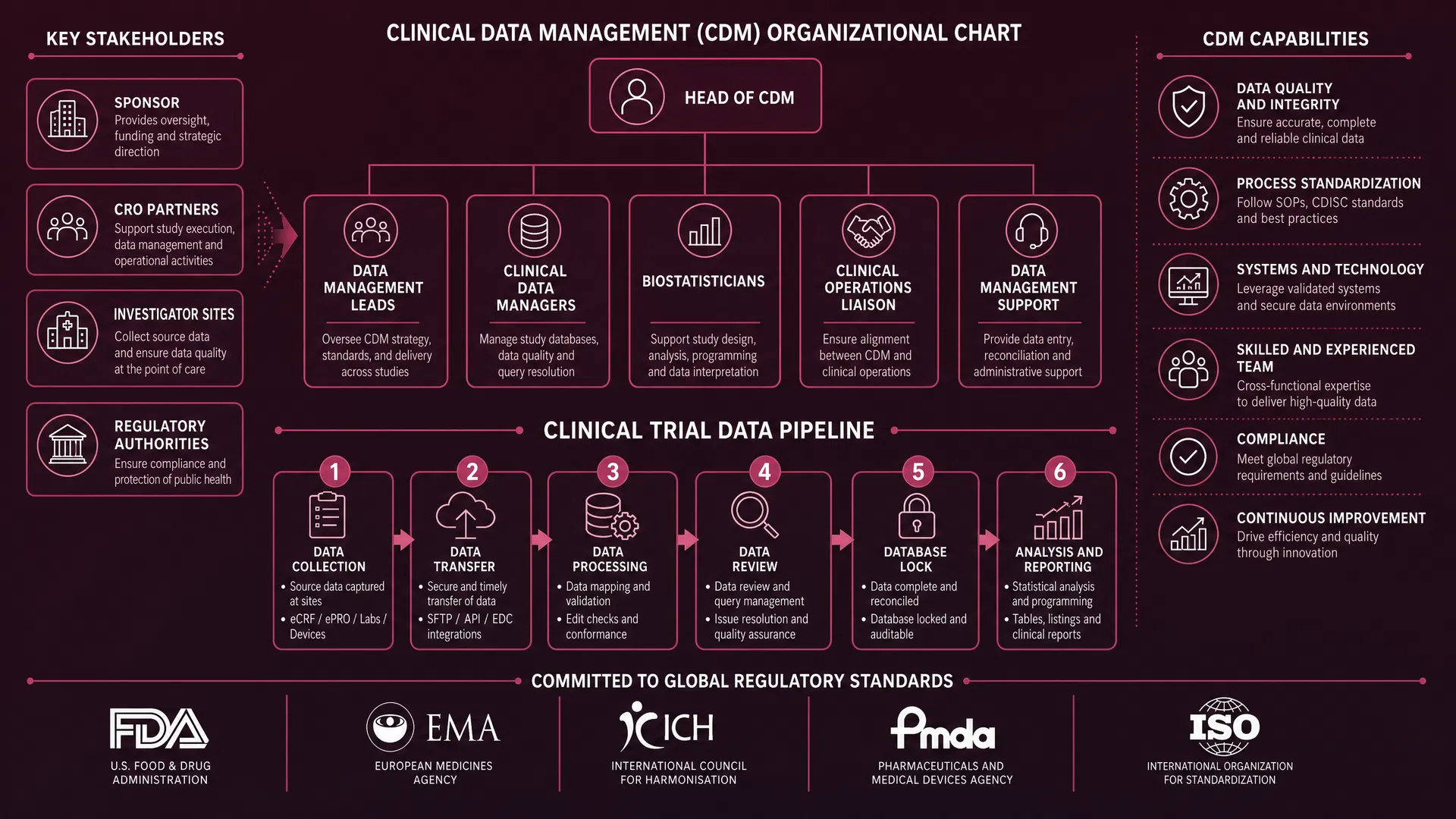
CDM ist eine kritische Phase in der Durchführung klinischer Studien. Es umfasst alle Prozesse zur systematischen Erfassung, Verwaltung und Qualitätssicherung von Studiendaten – von der Datenbankentwicklung bis zum finalen Database Lock.
Ziel des CDM ist es, sicherzustellen, dass die Daten einer klinischen Studie von höchster Qualität, Zuverlässigkeit und Gültigkeit sind. Nur auf Basis solcher Daten können valide Schlussfolgerungen über Wirksamkeit und Sicherheit eines Prüfpräparats gezogen werden.
DM-Teamstruktur: Sponsor vs. CRO
In globalen klinischen Studien ist das DM-Team typischerweise auf mehreren Ebenen organisiert. Die Zusammenarbeit zwischen Sponsor und CRO ist dabei entscheidend.
Sponsor-Seite
- Head of CDM
- Global Data Manager
- DM-Strategie & Oversight
CRO-Seite
- Lead Data Manager
- Lokale Data Manager
- Data Entry Specialists
Strategische Oversight, Standardisierung, Regulatory Submissions
Prüfstellen-Support, Query-Management, lokale Datenvalidierung
Wichtige DM-Deliverables
Das DM-Team ist für eine Reihe kritischer Dokumente und Artefakte verantwortlich, die den gesamten Studienzyklus begleiten.
Data Management Plan (DMP)
Das zentrale Steuerungsdokument des CDM. Beschreibt alle DM-Prozesse, Verantwortlichkeiten, Zeitpläne und Qualitätssicherungsmaßnahmen. Wird vor Studienbeginn erstellt und regelmäßig aktualisiert.
Trial Master File (TMF)
Vollständige Dokumentation aller wesentlichen Dokumente einer klinischen Studie gemäß ICH E6. Muss für Inspektionen durch Behörden (FDA, EMA) jederzeit verfügbar sein.
Cleaned Database
Die validierte, bereinigte Datenbank nach Database Lock. Grundlage für alle statistischen Analysen und behördlichen Einreichungen. Enthält alle Studiendaten in CDISC-konformem Format.
Data Validation Plan (DVP)
Definiert alle Edit Checks und Validierungsregeln für die Studie. Wird vom DM-Team in Abstimmung mit Biostatistik und Medical Affairs erstellt.
Schnittstellen des DM-Teams
Das DM-Team arbeitet eng mit verschiedenen Abteilungen zusammen. Jede Schnittstelle hat spezifische Anforderungen und Deliverables.
Biostatistik
SAP, TLFs, Database Lock
Clinical Operations
Monitoring, Site Management
Pharmakovigilanz
SAE-Reporting, MedDRA-Kodierung
Medical Affairs
Medical Review, Plausibilitätsprüfung
IT/Systeme
EDC-Validierung, Systemzugang
Regulatory Affairs
CDISC-Einreichungen, Behördenkommunikation
Regulatorische Grundlagen
GxP-Standards
GxP ist der Sammelbegriff für alle 'Good Practice'-Leitlinien: GCP (klinisch), GMP (Herstellung), GLP (Labor). Alle GxP-Standards fordern Datenintegrität, Rückverfolgbarkeit und Qualitätssicherung.
FDA 21 CFR Part 11
Die US-amerikanische FDA-Regulierung für elektronische Aufzeichnungen und Signaturen. Anforderungen: Audit Trail, Zugangskontrolle, elektronische Signaturen, Systemvalidierung und Datensicherung.
- Audit Trail (lückenlose Protokollierung)
- Zugangskontrolle (Rollen & Berechtigungen)
- Elektronische Signaturen (21 CFR Part 11.200)
- Systemvalidierung (IQ, OQ, PQ)
- Datensicherung & Disaster Recovery
ALCOA+ Prinzipien
ALCOA+ definiert die Qualitätsprinzipien für Daten in klinischen Studien:
Zuordenbar – Wer hat die Daten erstellt/geändert?
Lesbar – Daten müssen dauerhaft lesbar sein
Zeitnah – Daten zum Zeitpunkt der Erhebung erfassen
Ursprünglich – Erste Aufzeichnung oder zertifizierte Kopie
Korrekt – Fehlerfrei und wahrheitsgetreu
Vollständig, konsistent, dauerhaft, verfügbar
Interaktiver Datenfluss in klinischen Studien
Klicken Sie auf die einzelnen Schritte, um mehr über den Datenfluss zu erfahren.
Klicken Sie auf einen Schritt
Übung: DM-Organigramm
Ordnen Sie jede Rolle der richtigen Hierarchieebene zu. Wählen Sie für jede Rolle die passende Ebene aus.
Global Data Manager
Gesamtverantwortung für DM-Strategie und -Qualität
Lokaler Data Manager
Koordination auf Länderebene, Prüfstellen-Support
Data Entry Specialist
Dateneingabe und erste Plausibilitätsprüfung
Medical Coder
Kodierung von AEs mit MedDRA
Biostatistiker
Statistische Analyse, SAP, TLFs
Clinical Operations
Monitoring, Site Management, CRAs
Pharmakovigilanz
Sicherheitsüberwachung, SAE-Reporting
Wissenstest: Modul 1
Beantworten Sie alle 5 Fragen. Zum Bestehen sind 60% erforderlich.
Frage 1:Was ist die Hauptaufgabe des Clinical Data Managements (CDM)?
Frage 2:Welches Dokument beschreibt alle DM-Prozesse, Verantwortlichkeiten und Qualitätssicherungsmaßnahmen einer Studie?
Frage 3:Was regelt die FDA-Regulierung 21 CFR Part 11?
Frage 4:Was beschreibt das ALCOA+-Prinzip im Kontext der Datenintegrität?
Frage 5:Welche Schnittstelle hat das DM-Team typischerweise NICHT?